中国,已经成为真正的“胃癌大国”。
根据2020年全球癌症数据统计,我国胃癌新发患者有47.8万人,而全球范围同一时间新发胃癌人数是108.9万人,接近一半的胃癌患者都在中国。由于饮食习惯的不同,欧美国家,每10万人种只有6、7人患胃癌,而在中国每10万人种就有30人患胃癌。[1]
更令人忧虑的是,早在1984年,两名澳大利亚科学家发现:胃部感染幽门螺杆菌(HP),是引起胃炎、胃溃疡、胃癌等疾病的最主要原因,并因此获得诺贝尔医学奖。如今,幽门螺杆菌已经被世界卫生组织列为一级致癌物,感染幽门螺杆菌的人,胃癌发生率是普通人的6倍,目前国内幽门螺杆菌感染者已经超过5.6亿人![2]
幽门螺杆菌
氢氧混合气vs胃癌
在2007年日本学者研究发现:氢气可以选择性消除羟基自由基、并减轻了局部缺血再灌注引起的氧化应激和脑损伤之后[3],越来越多研究发现,氢气在预防和缓解不同癌症方面的潜力[4]:摄入氢气6周可以减少血液中的活性氧代谢物,维持血液氧化潜能,改善恶性肝癌患者放疗后的生活质量[5],持续3个月每天吸入氢氧气体,可以减少转移性胆囊癌,提高生活质量[6]。
因此,复旦大学中山医院的科学家进行了一项氢氧混合吸入抑制胃癌细胞增殖和迁移的实验,并在2021年将实验成果发表在国际期刊《Cancer Cell International》上。[7]
在该实验中,科学家购买人类胃癌细胞“MGC-803”、“BGC-823”,并在改良的培养基中进行培养。然后将这些胃癌细胞分为氢气组和对照组。其中,氢气组使用设备为获得“国家创新”三类医疗器械认证的潓美氢氧气雾化机(流量:3L/min;浓度:氢气66.6%,氧气33.3%)。

潓美氢氧气雾化机
氢氧抑制胃癌细胞增殖、迁移
由于氢气已被证明能抑制癌症进展[8]和肺癌细胞增殖[9],科学家首先研究了氢气是否会影响胃癌细胞的增殖。在氢氧混合气体暴露24小时后,与正常培养的MGC-803和BGC-823细胞相比,存活的MGC-803和BGC-823细胞减少了20%以上。
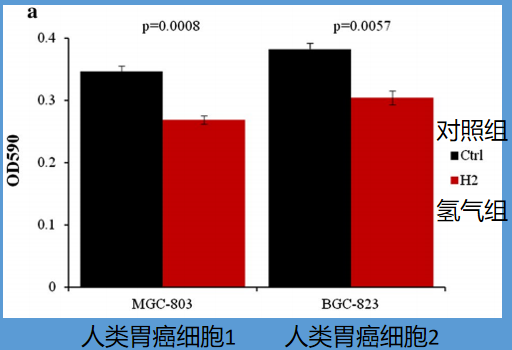
此外,氢氧混合气体使MGC-803细胞的运动能力显著降低约60%,使BGC-823细胞的运动能力显著降低50%以上。
科学家采用“划痕实验”来观测胃癌细胞的迁移:
科学家用尖锐工具在充斥胃癌细胞的培养板上划痕,显微镜下,划痕处无胃癌细胞,划痕两侧依旧充斥胃癌细胞。继续培养24小时之后,观察对照组、氢气组两边胃癌细胞“侵占”划痕处的速率,以此来评判胃癌细胞的运动能力。
该划痕实验对比结果非常显著,如下图:
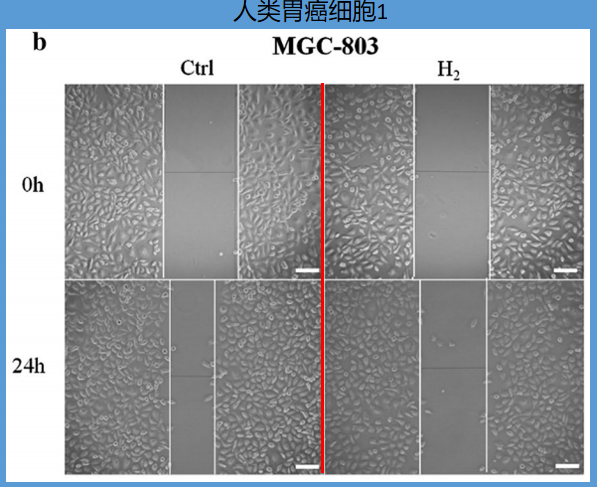
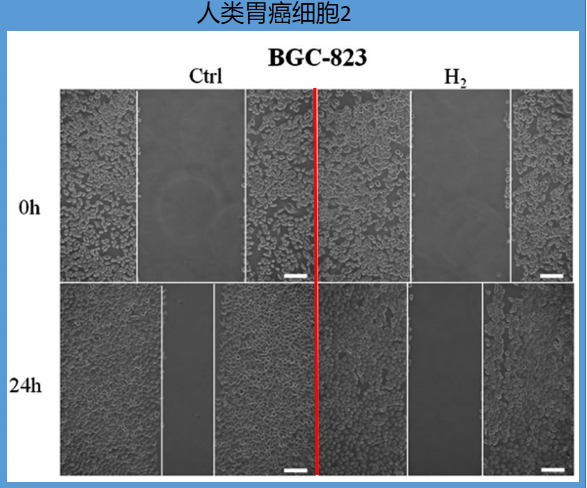
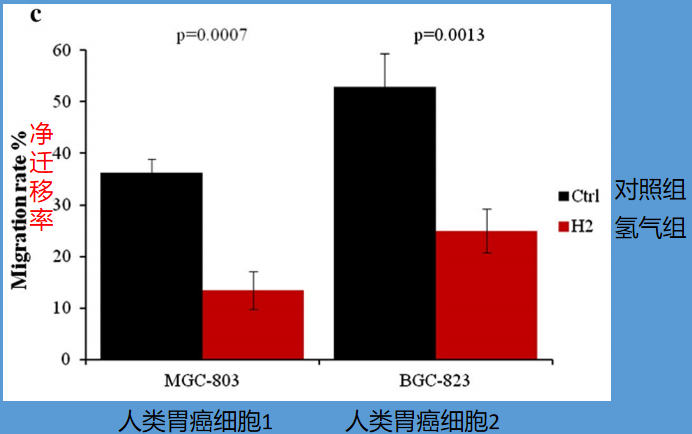
上调miR-124-3p抑制MALAT1
科学家还发现,氢气可以显著抑制胃癌细胞MGC-823中lncRNA MALAT1和转录因子EZH2的表达,同时上调miR-124-3p表达。
lncRNA是“长非编码”RNA(Long non-coding RNA),指的是超过200个核苷酸的非编码RNA。非编码RNA是不能翻译成蛋白质的RNA,非编码RNA自身就能发挥生物学作用。目前,发现非编码RNA表达或功能异常,与人类的疾病有密切关系,其中就包含退行性神经疾病(阿兹海默症等)以及癌症。
其中,本次实验涉及的IncRNA MALAT1已经被证明可促进癌细胞的增殖和迁移,上皮-间质转化和多种癌症类型的转移,可以增强胃癌细胞的干性、增殖、迁移、侵袭和耐药性。[10]
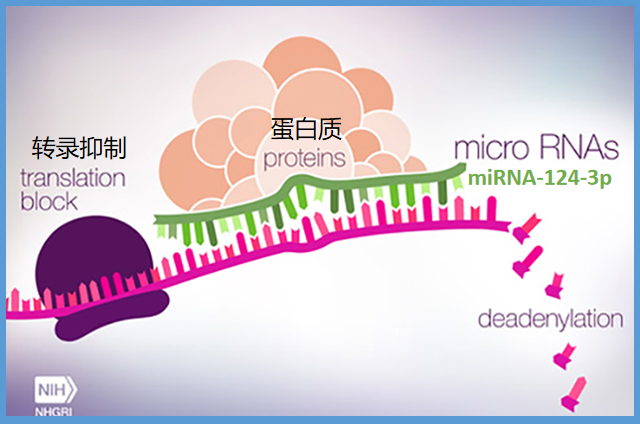
原本,科学研究中大分子(蛋白质、DNA)是被氢气影响的,在该实验中,我们发现小分子miRNA(一类由内源基因编码的长度约为22 个核苷酸的非编码单链RNA分子)也会被氢气影响。
miRNA(microRNA)是一类由内源基因编码的非编码单链RNA,主要通过参与基因的转录后调控实现对靶基因的表达调节。
miR-124-3p抑制EZH2表达,并与lncRNA MALAT1相互抑制表达,在抑制Slug表达和肝细胞癌转移方面也被lncRNA MALAT1拮抗。
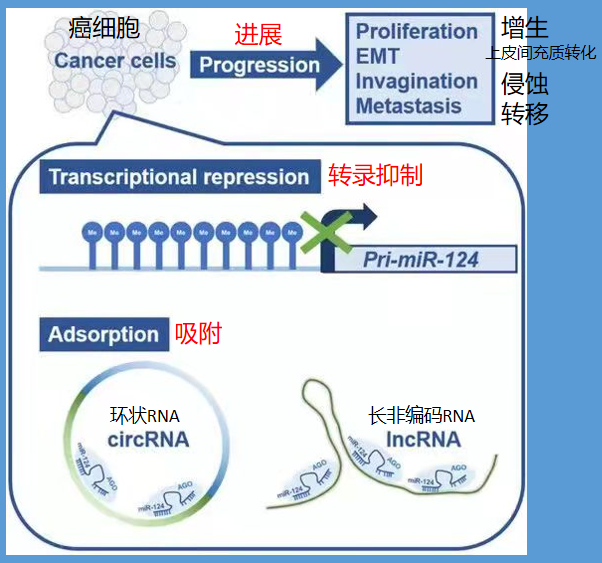
可以看到,miR-124可以“吸附”lncRNA,或可以抑制发挥生物学作用
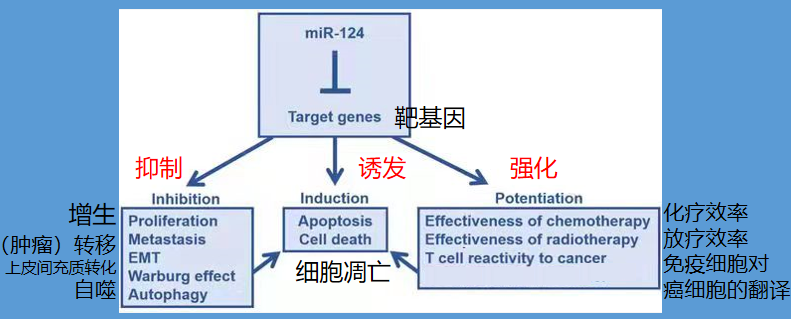
可以看到,miRNA是一种抑制癌症细胞的RNA,可以抑制癌症转移、增生,诱发癌症细胞凋亡、增强放化疗效率
miR-124-3p被鉴定为IncRNA MALAT1的靶点和调节因子。而H2可以上调miR-124-3p!
EZH2的突变或者过表达与多种类型癌症相关,如乳腺癌、前列腺癌、黑色素瘤和膀胱癌等。因为异常激活的EZH2可以抑制“抑癌基因”的正常表达,所以抑制EZH2的活性可以使肿瘤生长变慢。
EZH2的表达也被miR-124抑制。如下图:

miR-124 的靶基因和作用
又因为H2可以上调miR-124,H2环境下,EZH2和lncRNAMALAT1的表达都被抑制。
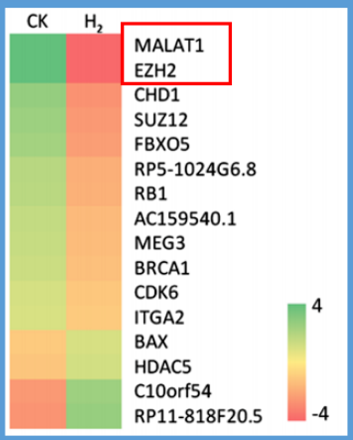
胃癌细胞对照组(CK)和氢气组(H2)基因组表达对比,抑制最明显的前两个基因分别是lncRNAMALAT1和EZH2。
miR-124-3p和MALAT1相互抑制
科学家还发现,miR-124-3p模拟物使两种胃癌细胞MGC-803和BGC-823的存活率降低20%以上(p<0.01,miR-124-3p与Ctrl相比)。
而lncRNA MALAT1对这两种胃癌细胞增殖的促进作用被miR-124-3p抑制(miR-124-3p+MALAT1与MALAT1相比,p<0.01,miR与miR-124-3p+MALAT1相比,p<0.01)如下:
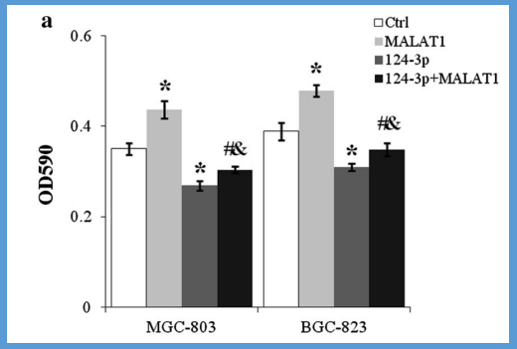
lncRNA MALAT1和miR-124-3p相互抑制
此外,miR-124-3p还抑制这两种胃癌细胞的迁移率约50%(p<0.01,miR-124-3p与Ctrl),并消除lncRNA MALAT1诱导的细胞运动性增加(miR-124-3p+MALAT1与MALAT1,以及miR-124-3p+MALAT1与miR-124-3p,p)如下:

-划痕实验的显著对比
吸入H2可显著抑制人类胃癌细胞在小鼠身上移植的肿瘤生长情况(p<0.01,H2与。Ctrl)这与不同癌症的临床观察结果一致。lncRNA MALAT1的过度表达部分抑制H2的作用,而miR-124-3p抵消了lncR MALAT1的作用。而H2可以上调miR-124-3p,所以得到实验结果:
H2+miR-124-3p>H2>H2+lncR MALAT1+miR-124-3p>H2+lncR MALAT1,结果如下:
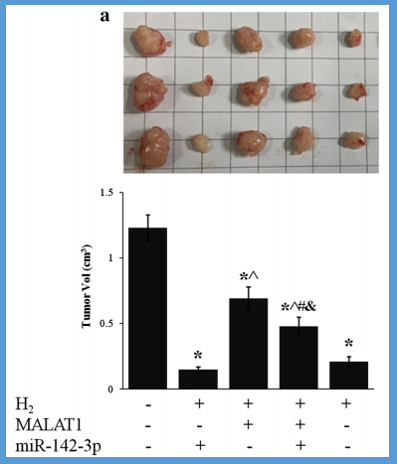
此外,H2暴露使miR-124-3p增强,胃肿瘤组织的EZH2蛋白水平降低50%以上,如下图:
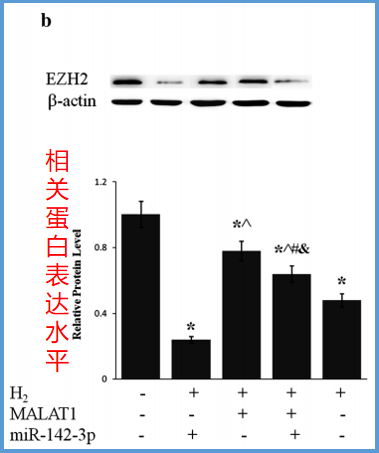
结果与讨论
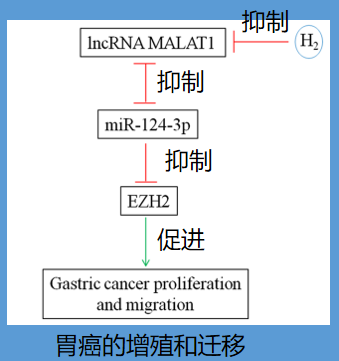
本研究证明了H2通过上调miR-124-3p,抑制lncRNA MALAT1,减少胃癌细胞的增殖和迁移,从而抑制胃癌的生长。miR-124-3p抑制EZH2表达,并与lncRNA MALAT1相互抑制表达。
这些数据表明,应进一步研究H2治疗胃癌,lncRNA MALAT1/miR-124-3p/EZH2轴可能是一个新的干预靶点。该实验证明了体外培育的人类胃癌细胞被H2控制,该结果为未来H2控制人类胃癌的临床实验打下基础。
这篇研究证明miR-124-3p可以成为治疗胃癌的标靶,而氢气可以直接影响内源性的miR-124-3p的表达。
注意:以上实验仅处于初步阶段,不可替代药物及专业医师指导,不具备临床指导意义。